キャッチアップ接種はどの程度の効果が期待できるのだろうか🐰オーストラリアのケースを例に
オーストラリアでは2007年にHPVワクチンが導入され2009年まで26歳までを対象にキャッチアップ接種が行われた。接種対象と接種率、初交年齢の中央値をまとめたのがこれ。

(公表されている最新の子宮頸がん罹患率である)2019年において30代は性的デビュー後にワクチンを接種したいわゆるキャッチアップ世代で構成されているのがわかるだろう。
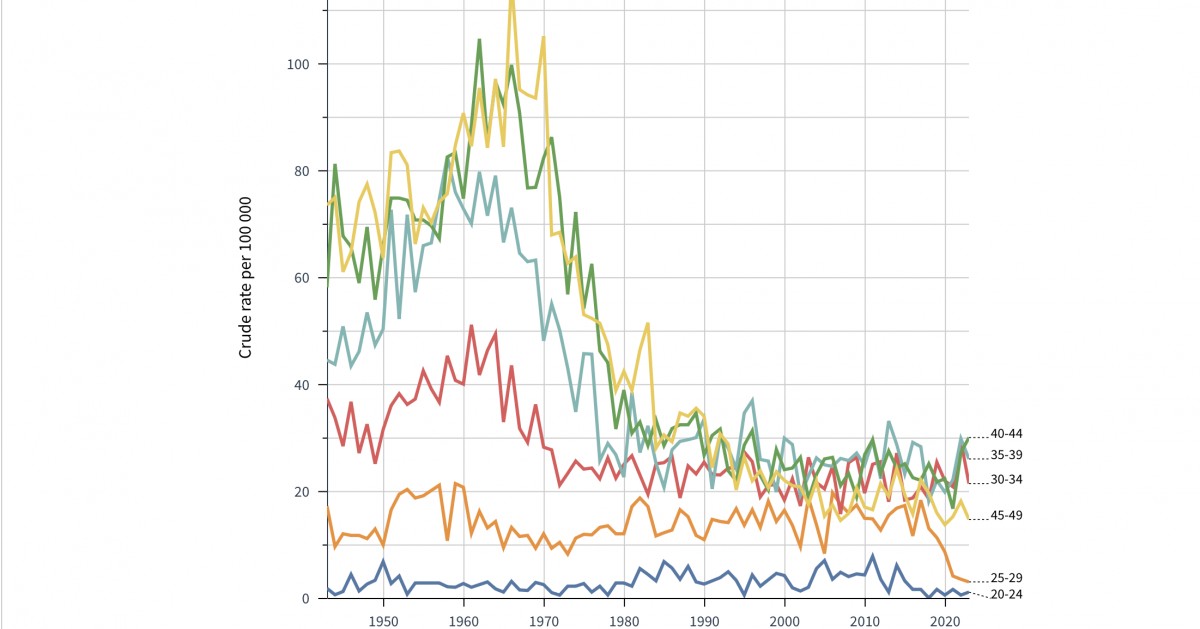
ワクチン接種開始2007年以降の20代・30代の子宮頸がん罹患率をそれぞれ見てみよう(水色の一番右端が2019年の数値だ)。

30代のデータ。罹患率は2000年以降増加傾向にあり、ワクチン接種でトレンドの変化はない。

20代のデータ。2000年以降増加傾向になるが、ワクチン接種集団で置き換えが進む2013年以降子宮頸がんが急減している。
簡単に解説すると
-
多くが性的にデビュー後であったキャッチアップ接種対象者は60%近い接種率があったにもかかわらず、2019年時点で子宮頸がんが減っていない(30代)。
-
多くが性的デビュー前であった定期接種対象者は、接種率が高かったこともあり、209年時点で子宮頸がんが激減している(20代)
ざっくりまとめると『HPVワクチンはタイミングが重要。なるべく若い時に接種したほうがいい』ということだ。
では、キャッチアップ接種は全く意味がないのだろうか?
そんなことはない。
『子宮頸がん予防効果は期待されているが、明らかになるにはさらに時間がかかる』とされている。説明しよう🐰
まずHPV感染から子宮頸がん発症までの自然史を知ろう
HPV感染から子宮頸がん発症までは中央値で10年以上・数十年かかることもある。
-
ハイリスクHPVへの感染は性的デビュー後比較的速やかに起こる。
-
感染後一番最初の変化は『HPV検査の陽性化』になる。感染後すぐに陽性になる可能性があり。前がん病変がある様な感染ではほ100%陽性になる(感度が高い)。20代でスクリーニングとして検査されることはないので、知られないことがほとんどだ。
-
次に感染病変(異形成・前がん病変)が形成される。感染後数ヶ月から起こってもよく、5〜10年後にかけてピークがある。
-
最後に一部が『がん』としての発症する。英国の統計を借りれば、感染機会から8年以内にがんが発症することはほとんどなく。中央値は10〜15年。その後もだらだらと発症している。
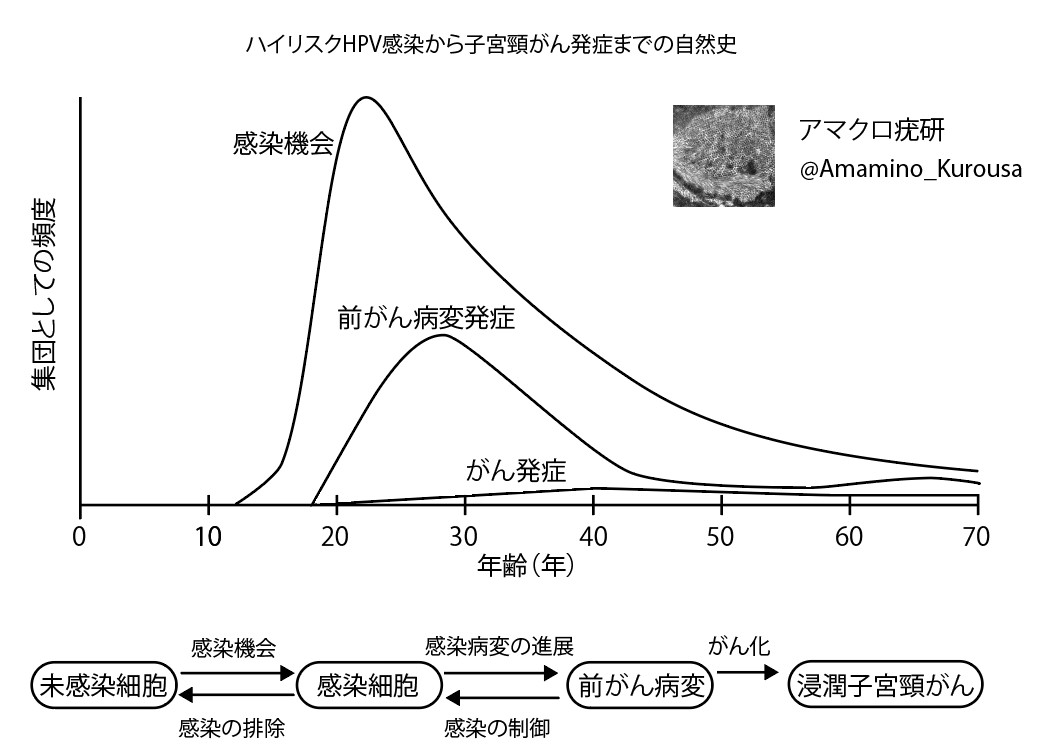
疫学調査でわかっていること。感染の排除が起こるのか、起こるとしてどの程度起こるのかわからない。
ここで大事なのは、HPVワクチンを接種して感染予防効果があったとして、それが確認されるようになるのは①HPV検査の陽性率としては数年②前がん病変の発症としては数年〜10数年③がんの発症としては15年から数十年と、感染からのタイムラグに応じて時間がかかることだ。
HPVワクチンは完全な感染予防ワクチンなので、接種以前に感染していたものには効果がない。つまり、感染機会があったキャッチアップ接種対象者からは接種後も接種前の感染が原因となるHPV陽性・前がん病変の発症・がんの発症が同じ数起こる。
もちろん、接種後の感染が原因となるHPV陽性・前がん病変の発症・がんの発症は減少することが期待できる。それが見えるようになるまでには、HPV陽性なら数年・前がん病変の発症なら5年以上・がんの発症であれば20年近くかかるだろう。
定期接種集団とのちがいは、接種時に既にいくつかのハイリスクHPVに感染しているかどうかの違いだ。定期接種者は接種時には感染していないことが期待できるので、将来発症する子宮頸がんのうち『ワクチンの標的となるものは全て予防できる』と期待できるが、キャッチアップ対象者は『ワクチンの標的となるものから既感染のものを除いて予防できる』となる。
2019年の30代の子宮頸がんはワクチン接種前に感染したものが原因になっているということだ🐰(残念だ)『③がんの発症としては15年から数十年』かかるのだから当然のこと。
では、ワクチン接種後の感染に関しては効果があるとどうして言えるのか?
HPV検査の陽性率の減少・前がん病変の発症率の減少として予防効果が確認されている。
臨床試験において、既感染者においても『感染しているのとは別の型のHPV』が感染するのを予防できた結果、前がん病変の罹患率がへることがわかっている。同時に複数のHPVに感染することが極々普通のことであることを示唆するデータでもある。
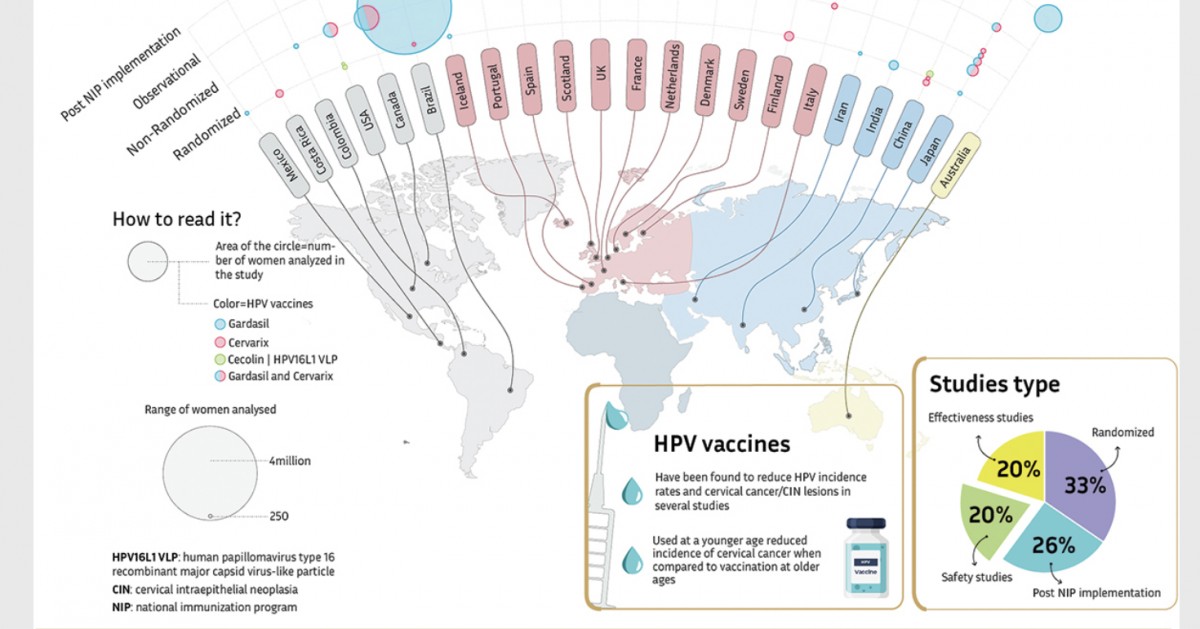
実社会のデータではどうか?それを示すのが今日の論文。オープンアクセスだよ🐰
DOI: 10.1016/j.lanwpc.2021.100251
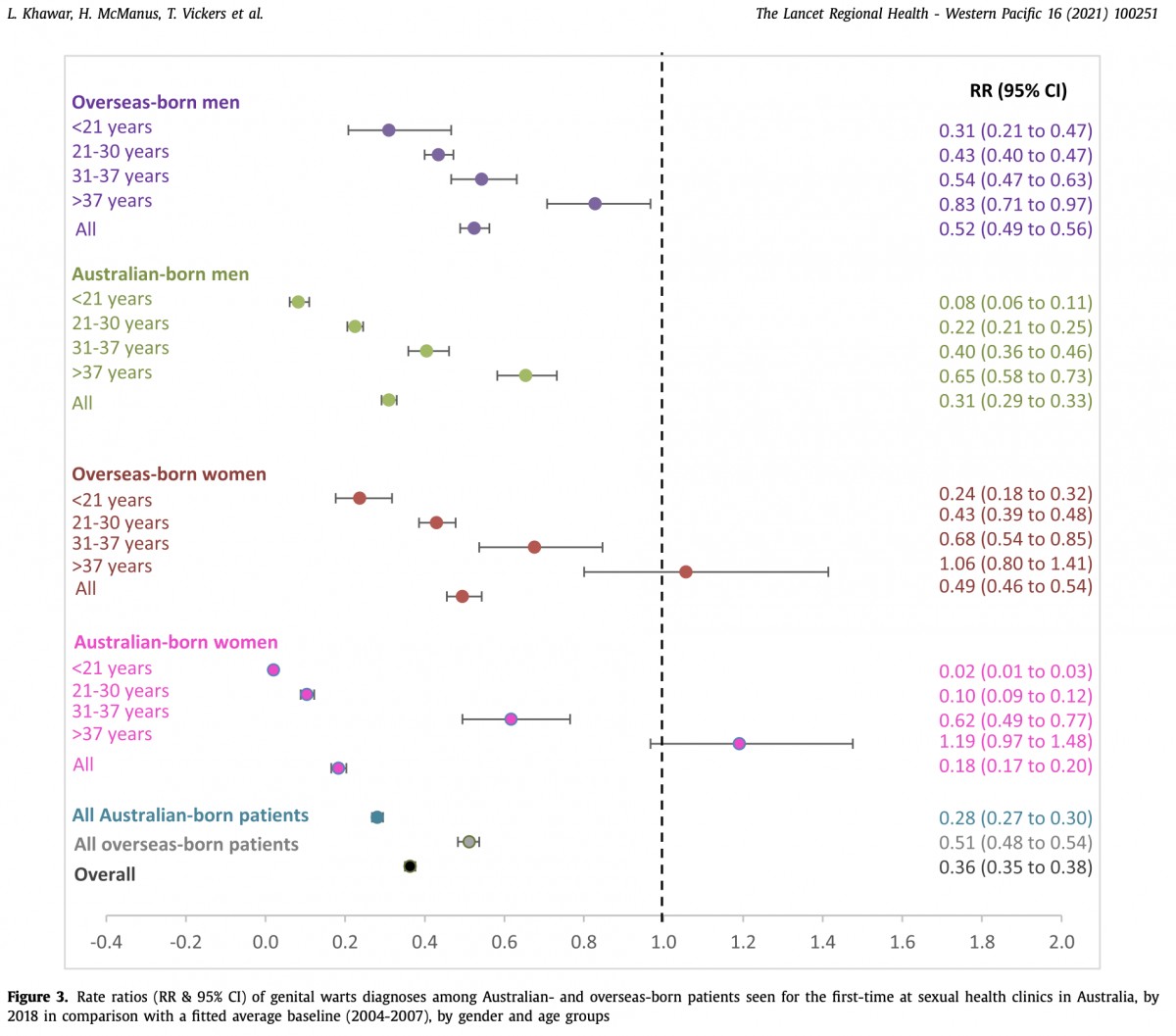
オーストラリア全体で、尖圭コンジローマの罹患率(尖圭コンジローマと診断された数)をワクチンの対象世代前後で比較したものになる。ここでは上から4つ目のピンクだけに注目してほしい。ワクチン導入前(2004-7年)を基準に、2018年の各世代(20歳以下・20代・30代に分けてある。2018年時点で37歳以下がワクチンの対象であった)のコンジローマ罹患率の変化を示したものだ。
・20歳以下のコンジローマは消滅した。
・定期接種を受けた集団・20代のコンジローマは9割減った。
・キャッチアップ接種対象であった2018年の30代のコンジローマも4割減った。
コンジローマの発症は、先に説明したHPV感染の3症候①HPV検査の陽性②前がん病変の発症③がんの発症のうち、②の前がん病変・異形成の形成と同等のことになる。つまり、リアルワールドのデータにおいてもHPVの感染の予防による異形成の予防が数値として確認されているということね🐰
接種前の感染が原因のがんの罹患は減っていないが、接種後感染機会が原因となるはずだった異形成の形成は予防できている。だから、接種後感染機会による異形成が原因となるはずだった『がん発症』が予防できることが期待されているというわけ。
40代以降の子宮頸がん減少として出てくると推定されるのだけど、🐰にはどの程度減少すると推定されるのが妥当かに関しての判断に自信がない。モデル計算はなされているが、これこそ実際の数値が出てくることによって正しく評価されるでしょう。
蛇足:全体でみてもワクチン導入以降2018年の時点でコンジローマが8割以上減少している。コンジローマの罹患ピークは子宮頸部の異形成と同様で20代後半から35歳あたりにあるから、その多くがワクチンを接種していることになるからだ。ざっくり『オーストラリアでは、尖圭コンジローマはワクチンを接種していない人の病気となった』と言える🐰すごくない?
まとめ
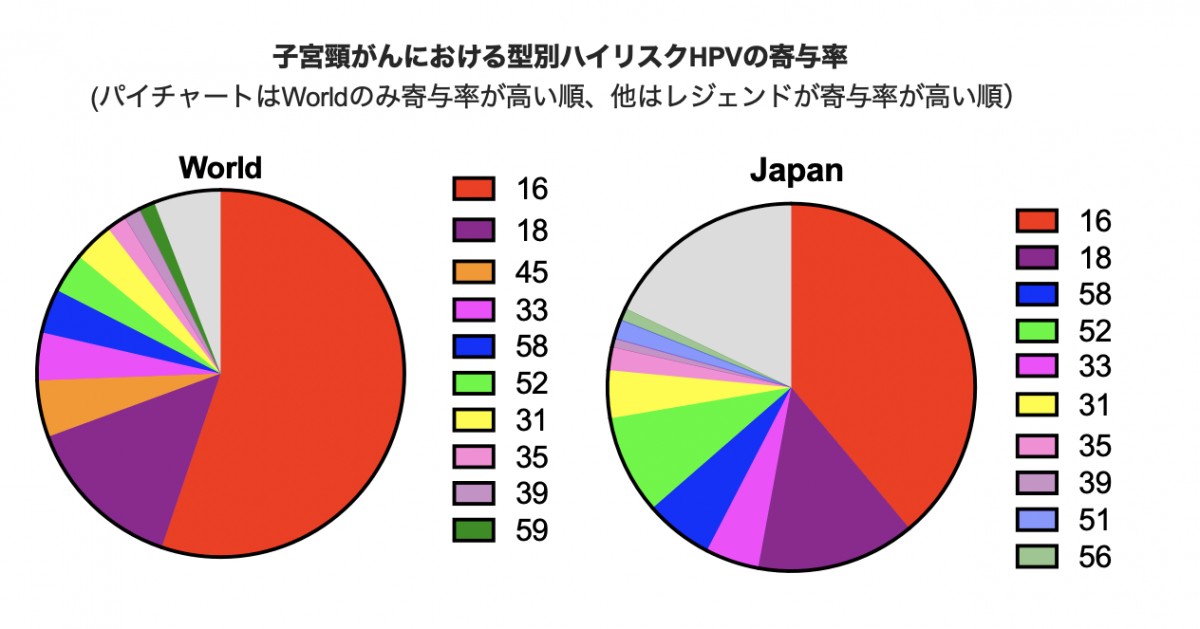
オーストラリアのデータを見ると、30代の子宮頸がんは、ワクチン接種前(26歳以前)に感染したハイリスクHPV特にHPV16・18によるものであることがわかる。キャッチアップ接種対象者は特に検診の重要性が強調される。30代に発症する子宮頸がんはワクチン接種でほとんど減らないので徹底した検診で予防することが必要だ。
キャッチアップ接種の子宮頸がん予防効果が疫学的に見えるようになるのは、少なくとも40歳以降になるだろう。それでも、相当数の子宮頸がんがワクチンで予防できると期待できるし、検診を受ける上での実質的な負担である前がん病変はさらに予防できることがわかっている。
キャッチアップ接種プログラムの実施期間は来年度までだ。ワクチンの効果は確実にあるので、期待するのであればなるべく早く接種したほうがいいだろう。
すでに登録済みの方は こちら